REAKSI RADIKAL BEBAS
REAKSI RADIKAL BEBAS
 |
Radikal bebas adalah atom atau gugus atom apa saja yang memiliki satu atau lebih elektron tidak berpasangan. Maksudnya jumlah elektron dalam atom atau gugus atom tersebut ganjil, sehingga tidak semuanya yang bisa berpasangan.
Molekul radikal tidak disebut bermuatan positif atau negatif, tetapi ia menjadi sangat reaktif karena adanya elektron tidak berpasangan ini. Untuk menulis lambang bahwa suatu atom atau gugus atom adalah radikal bebas, maka elektron tidak berpasangan ini dilambangkan dengan satu titik.
Radikal bebas adalah suatu molekul atau ion yang mengandung satu elektron yang tidak berpasangan. Merupakan juga suatu kelompok bahan kimia dengan reaksi jangka pendek yang memiliki satu atau lebih elektron bebas. Senyawa ini merupakan zat antara yang berusia pendek, sangat reaktif dan berenergi tinggi, sehingga memiliki kecenderungan menarik elektron dari molekul lainnya dan memicu reaksi berantai (Evans, 1991; Kardinaal, 1994). Radikal bebas dihasilkan dari pemutusan ikatan kovalen secara homolitik dimana terbentuk dua fragmen yang memiliki elektron tak berpasangan dan bersifat radikal (Frei, 1994). Radikal bebas dapat bersifat anonik, kationik, atau netral (Punchard, 1996). Fungsi radikal bebas diantaranya membunuh bakteri intraseluler. Bila terdapat radikal bebas di dalam tubuh secara berlebih maka akan terjadi perampasan elektron atom komponen struktral maupun fungsional sel kemudian terjadi reaksi berantai (Niwa, 1997).
Contoh :
Tulislah rumus lewis untuk radikal bebas :
Tanda titik pada rumus diatas menandakan elektron tidak berpasangan pada gugus atom radikal bebas. Rumus diatas disebut dengan rumus biasa untuk radikal bebas.
Untuk membuat rumus lewisnya tinggal ditampakkan semua elektron berpasangan dari atom – atom pada gugus atom diatas.
Untuk membuat rumus lewisnya tinggal ditampakkan semua elektron berpasangan dari atom – atom pada gugus atom diatas.

Salah satu reaksi radikal bebas yang paling umum adalah reaksi klorinasi metana dengan bantuan cahaya ultra violet (hν). Reaksi terjadi antara Cl2 dengan metana (CH4) dimana salah satu atau lebih atom H pada metana diganti oleh atom Cl dari Cl2. Reaksi ini sering juga disebut reaksi substitusi radikal bebas.
Oleh karena bisa lebih dari satu atom H metana yang dapat digantikan oleh Cl2 maka produk klorinasi metana adalah campuran dari empat senyawa sesuai dengan reaksi berikut :
CH4 + Cl2 ==> CH3Cl + CH2Cl2 + CHCl3 + CCl4 + HCl
Produk 1 2 3 4
Reaksi radikal bebas klorinasi metana (dan juga reaksi radikal bebas yang lain) berlangsung melalui tiga tahap mekanisme yaitu sebagai berikut :
Inisiasi
Pada tahap ini terjadi pembentukan awal radikal bebas dimana terjadi pemaksapisahan homolitik molekul Cl2 membentuk dua buah atom Cl radikal. Reaksi ini terjadi pada suhu yangsangat tinggi.
Oleh karena bisa lebih dari satu atom H metana yang dapat digantikan oleh Cl2 maka produk klorinasi metana adalah campuran dari empat senyawa sesuai dengan reaksi berikut :
CH4 + Cl2 ==> CH3Cl + CH2Cl2 + CHCl3 + CCl4 + HCl
Produk 1 2 3 4
Reaksi radikal bebas klorinasi metana (dan juga reaksi radikal bebas yang lain) berlangsung melalui tiga tahap mekanisme yaitu sebagai berikut :
Inisiasi
Pada tahap ini terjadi pembentukan awal radikal bebas dimana terjadi pemaksapisahan homolitik molekul Cl2 membentuk dua buah atom Cl radikal. Reaksi ini terjadi pada suhu yangsangat tinggi.
Propagasi
Setelah radikal bebas baru terbentuk, maka reaksi pembentukan radikal bebas lain juga akan terjadi sehingga gugus atom dan gugus atom radikal bebas menjadi banyak. Inilah yang disebut dengan tahap propagasi.
Pada reaksi klorinasi metana, radikal Cl merebut atom H dari metanan sehingga terbentuk radikal bebas metil dan HCl.
Reaksi yang terjadi :
Metil radkal yang terbentuk juga reaktif dan akan merebut atom Cl dari Cl2 yang lain. Ini adalah tahap propagasi kedua.
Pada tahap propagasi kedua ini, produk 1 sudah terbentuk yaitu CH3Cl.
Produk ini akan merebut kembali atom Cl dari Cl2 lainnya sehingga membentuk Cl radikal bebas. Cl radikal bebas yang terbentuk juga akan merebut atom H dari molekul metana yang lain sehingga terjadi lagi deret propagasi yang lain.
Selagi molekul molekul yang dibutuhkan dalam reaksi tersedia, reaksi propagasi ini akan terus menerus berulang. Banyaknya reaksi propagasi yang terjadi pada suatu reaksi radikal bebas disebut panjang rantai.
Untuk klorinasi suatu molekul hidrokarbon panjang rantainya adalah sekitar 10.000 yangartinya terjadi 10.000 kali pengulangan tahap propagasi.
Terminasi
Terminasi adalah tahap terakhir dari reaksi radikal bebas dimanan rantai popagasinya diputus oleh zat apa apa saja yang dapat mengubah molekul radikal bebas yang terbentuk menjadi stabil.
Reaksi radikal bebas klorinasi metana diputus oleh penggabungan dua molekul radikal bebas sehingga menjadi molekul yang tidak reaktif.
- Struktur Kimia Radikal Bebas
Atom terdiri dari nukleus, proton, dan elektron. Jumlah proton (bermuatan positif) dalam nukleus menentukan jumlah dari elektron (bermuatan negatif) yang mengelilingi atom
tersebut. Elektron berperan dalam reaksi kimia dan merupakan bahan yang menggabungkan atom-atom untuk membentuk suatu molekul. Elektron mengelilingi, atau mengorbit suatu atom dalam satu atau lebih lapisan. Jika satu lapisan penuh, elektron akan mengisi lapisan kedua. Lapisan kedua akan penuh jika telah memiliki 8 elektron, dan seterusnya.
Gambaran struktur terpenting sebuah atom dalam menentukan sifat kimianya adalah jumlah elektron pada lapisan luarnya. Suatu bahan yang elektron lapisan luarnya penuh tidak akan terjadi reaksi kimia. Karena atom-atom berusaha untuk mencapai keadaan stabilitas maksimum, sebuah atom akan selalu mencoba untuk melengkapi lapisan luarnya dengan :
a. Menambah atau mengurangi elektron untuk mengisi maupun mengosongkan
lapisan luarnya.
b. Membagi elektron-elektronnya dengan cara bergabung bersama atom yang lain dalam rangka melegkapi lapisan luarnya.
Atom sering kali melengkapi lapisan luarnya dengan cara membagi elektron-elektron
bersama atom yang lain. Dengan membagi elektron, atom-atom tersebut bergabung bersama dan mencapai kondisi stabilitas maksimum untuk membentuk molekul. Oleh karena radikal bebas sangat reaktif, maka mempunyai spesifitas kimia yang rendah sehingga dapat bereaksi dengan berbagai molekul lain, seperti protein, lemak, karbohidrat, dan DNA.
Dalam rangka mendapatkan stabilitas kimia, radikal bebas tidak dapat mempertahankan bentuk asli dalam waktu lama dan segera berikatan dengan bahan sekitarnya. Radikal bebas akan menyerang molekul stabil yang terdekat dan mengambil elektron, zat yang terambil elektronnya akan menjadi radikal bebas juga sehingga akan memulai suatu reaksi berantai, yang akhirnya terjadi kerusakan sel tersebut.
 |
Gambar 1. Struktur kimia radikal bebas
Radikal bebas dapat terbentuk in-vivo dan in-vitro secara :
- Pemecahan satu molekul normal secara homolitik menjadi dua. Proses ini jarang terjadi pada sistem biologi karena memerlukan tenaga yang tinggi dari sinar ultraviolet, panas, dan radiasi ion.
- Kehilangan satu elektron dari molekul normal
- Penambahan elektron pada molekul normal
Pada radikal bebas elektron yang tidak berpasangan tidak mempengaruhi muatan elektrik dari molekulnya, dapat bermuatan positif, negatif, atau netral.
III. Tipe radikal bebas dalam tubuh
Radikal bebas terpenting dalam tubuh adalah radikal derivat dari oksigen yang disebut
kelompok oksigen reaktif (reactive oxygen species/ROS), termasuk didalamnya adalah triplet (3O2), tunggal (singlet/1O2), anion superoksida (O2.-), radikal hidroksil (-OH), nitrit oksida (NO-), peroksinitrit (ONOO-), asam hipoklorus (HOCl), hidrogen peroksida (H2O2), radikal alkoxyl (LO-), dan radikal peroksil (LO-2).
Radikal bebas yang mengandung karbon (CCL3-) yang berasal dari oksidasi radikal
molekul organik. Radikal yang mengandung hidrogen hasil dari penyerangan atom H (H-). Bentuk lain adalah radikal yang mengandung sulfur yang diproduksi pada oksidasi glutation menghasilkan radikal thiyl (R-S-). Radikal yang mengandung nitrogen juga ditemukan, misalnya radikal fenyldiazine.
 |
IV. Sumber radikal bebas
Radikal bebas yang ada ditubuh manusia berasal dari 2 sumber :
- Endogen
- Eksogen
a. Sumber endogen
1. Autoksidasi
Merupakan produk dari proses metabolisme aerobik. Molekul yang mengalami autoksidasi berasal dari katekolamin, hemoglobin, mioglobin, sitokrom C yang tereduksi, dan thiol. Autoksidasi dari molekul diatas menghasilkan reduksi dari oksigen diradikal dan pembentukan kelompok reaktif oksigen. Superoksida merupakan bentukan awal radikal. Ion ferrous (Fe II) juga dapat kehilangan elektronnya melalui oksigen untuk membuat superoksida dan Fe III melalui proses autoksidasi.
2. Oksidasi enzimatik
Beberapa jenis sistem enzim mampu menghasilkan radikal bebas dalam jumlah yang cukup bermakna, meliputi xanthine oxidase (activated in ischemiareperfusion), prostaglandin synthase, lipoxygenase, aldehyde oxidase, dan amino acid oxidase. Enzim myeloperoxidase hasil aktifasi netrofil, memanfaatkan hidrogen peroksida untuk oksidasi ion klorida menjadi suatu oksidan yang kuat asam hipoklor.
3. Respiratory burst
Merupakan terminologi yang digunakan untuk menggambarkan proses dimana sel fagositik menggunakan oksigen dalam jumlah yang besar selama fagositosis. Lebih kurang 70-90 % penggunaan oksigen tersebut dapat diperhitungkan dalam produksi superoksida. Fagositik sel tersebut memiliki sistem membran bound flavoprotein cytochrome-b-245 NADPH oxidase. Enzim membran sel seperti NADPH-oxidase keluar dalam bentuk inaktif. Paparan terhadap bakteri yang diselimuti imunoglobulin, kompleks imun, komplemen 5a, atau leukotrien dapat mengaktifkan enzim NADPH-oxidase. Aktifasi tersebut mengawali respiratory dibentuk dari superoksida dengan cara dismutasi bersama generasi berikutnya dari OH dan HOCl oleh bakteri.
b. Sumber eksogen
1. Obat-obatan
Beberapa macam obat dapat meningkatkan produksi radikal bebas dalam bentuk peningkatan tekanan oksigen. Bahan-bahan tersebut bereaksi bersama hiperoksia dapat mempercepat tingkat kerusakan. Termasuk didalamnya antibiotika kelompok quinoid atau berikatan logam untuk aktifitasnya (nitrofurantoin), obat kanker seperti bleomycin, anthracyclines (adriamycin), dan methotrexate, yang memiliki aktifitas pro-oksidan. Selain itu, radikal juga berasal dari fenilbutason, beberapa asam fenamat dan komponen aminosalisilat dari sulfasalasin dapat menginaktifasi protease, dan penggunaan asam askorbat dalam jumlah banyak mempercepat peroksidasi lemak.
2. Radiasi
Radioterapi memungkinkan terjadinya kerusakan jaringan yang disebabkan oleh radikal bebas. Radiasi elektromagnetik (sinar X, sinar gamma) dan radiasi partikel (partikel elektron, photon, neutron, alfa, dan beta) menghasilkan radikal primer dengan cara memindahkan energinya pada komponen seluler seperti air. Radikal primer tersebut dapat mengalami reaksi sekunder bersama oksigen yang terurai atau bersama cairan seluler.
3. Asap rokok
Oksidan dalam rokok mempunyai jumlah yang cukup untuk memainkan peranan yang besar terjadinya kerusakan saluran napas. Telah diketahui bahwa oksidan asap tembakau menghabiskan antioksidan intraseluler dalam sel paru (in vivo) melalui mekanisme yang dikaitkan terhadap tekanan oksidan. Diperkirakan bahwa tiap hisapan rokok mempunyai bahan oksidan dalam jumlah yang sangat besar, meliputi aldehida, epoxida, peroxida, dan radikal bebas lain yang mungkin cukup berumur panjang dan bertahan hingga menyebabkan kerusakan alveoli. Bahan lain seperti nitrit oksida, radikal peroksil, dan radikal yang mengandung karbon ada dalam fase gas. Juga mengandung radikal lain yang relatif stabil dalam fase tar.
Contoh radikal dalam fase tar meliputi semiquinone moieties dihasilkan dari bermacam-macam quinone dan hydroquinone. Perdarahan kecil berulang merupakan penyebab yang sangat mungkin dari desposisi besi dalam jaringan paru perokok. Besi dalam bentuk tersebut meyebabkan pembentukan radikal hidroksil yang mematikan dari hidrogen peroksida. Juga ditemukan bahwa perokok mengalami peningkatan netrofil dalam saluran napas bawah yang mempunyai kontribusi pada peningkatan lebih lanjut konsentrasi radikal bebas.
V. Pembentukan radikal bebas dalam sel
Radikal bebas diproduksi dalam sel yang secara umum melalui reaksi pemindahan elektron, menggunakan mediator enzimatik atau non-enzimatik. Produksi radikal bebas dalam sel dapat terjadi secara rutin maupun sebagai reaksi terhadap rangsangan. Secara rutin adalah superoksida yang dihasilkan melalui aktifasi fagosit dan reaksi katalisa kebocoran superoksida, hidrogen peroksida dan kelompok oksigen reaktif (ROS) lainnya pada saat bertemunya bakteri dengan fagosit teraktifasi. Pada keadaan normal sumber utama radikal bebas adalah kebocoran elektron yang terjadi dari rantai transport elektron, misalnya yang ada dalam mitokondria dan endoplasma retikulum dan molekul oksigen yang menghasilkan superoksida. Dalam kondisi yang tidak lazim seperti radiasi ion, sinar ultraviolet, dan paparan energi tinggi lainnya, dihasilkan radikal bebas yang sangat berlebihan.
 |
VI. Reaksi perusakan oleh radikal bebas
Definisi tekanan oksidatif (oxidative stress) adalah suatu keadaan dimana tingkat oksigen reaktif intermediate (ROI) yang toksik melebihi pertahanan anti-oksidan endogen. Keadaan ini mengakibatkan kelebihan radikal bebas, yang akan bereaksi dengan lemak, protein, asam nukleat seluler, sehingga terjadi kerusakan lokal dan disfungsi organ tertentu. Lemak merupakan biomolekul yang rentan terhadap serangan radikal bebas.
a. Peroksidasi lemak
Membran sel kaya akan sumber poly unsaturated fatty acid (PUFA), yang mudah dirusak oleh bahan-bahan pengoksidasi; proses tersebut dinamakan peroksidasi lemak. Hal ini sangat merusak karena merupakan suatu proses berkelanjutan. Pemecahan hidroperoksida lemak sering melibatkan katalisis ion logam transisi.
b. Kerusakan protein
Protein dan asam nukleat lebih tahan terhadap radikal bebas daripada PUFA, sehingga kecil kemungkinan dalam terjadinya reaksi berantai yang cepat. Serangan radikal bebas terhadap protein sangat jarang kecuali bila sangat ekstensif. Hal ini terjadi hanya jika radikal tersebut mampu berakumulasi (jarang pada sel normal), atau bila kerusakannya terfokus pada daerah tertentu dalam protein. Salah satu penyebab kerusakan terfokus adalah jika protein berikatan dengan ion logam transisi.
c. Kerusakan DNA
Seperti pada protein kecil kemungkinan terjadinya kerusakan di DNA menjadi suatu reaksi berantai, biasanya kerusakan terjadi bila ada lesi pada susunan molekul, apabila tidak dapat diatasi, dan terjadi sebelum replikasi maka akan terjadi mutasi. Radikal oksigen dapat menyerang DNA jika terbentuk disekitar DNA seperti pada radiasi biologis.
VIII. Pertahanan sel terhadap radikal bebas
Sifat reaktif yang tersebar dari sistem pembentukan radikal dalam sel menyebabkan evolusi mekanisme pertahanan terhadap efek perusakan suatu bahan teroksidasi kuat. Gambar dibawah ini menunjukkan aktifitas enzim intraseluler tersebut. SOD (superoksida dismutase dan katalase) mengkatalisasi dismutasi dari superoksida dan hidrogen peroksida. GSH (glutation) peroksidase mereduksi peroksida hidrogen dan organik menjadi air dan alkohol. GSH S-transferase melakukan pemindahan residu glutation menjadi metabolit elektrofilik reaktif dari xenobiotic. Produksi glutation teroksidasi (GSSG) direduksi secara cepat oleh reaksi yang menggunakan NADPH yang dihasilkan dari berbagai sistem intraseluler, diantaranya hexose-monophosphate shunt. Berbagai isoenzim organel spesifik dari dismutase superoksida juga ditemukan. SOD Zn, Cu merupakan sitoplasmik, sedangkan enzim Zn, Mn mitokondrial. Isoenzim ini tidak ditemukan dalam cairan ekstraseluler.
 |
| Gambar 3. Enzim-enzim pertahanan antioksidan |
Beberapa bahan tereduksi juga bekerja sebagai antioksidan, reduksi kelompok radikal aktif seperti radikal peroksi dan hidroksi menjadi bentuk yang kurang reaktif misalnya air. Seperti halnya pembangkitan kembali oksigen singlet. Penggabungan tersebut juga mengakhiri reaksi radikal berantai. Pertahanan antioksidan kimiawi bagai pedang bermata dua. Pertama, saat bahan tereduksi menjadi radikal maka derivat radikalnya juga terbentuk. Sehingga, jika suatu radikal sangat tidak stabil, reaksi radikal berantai mungkin akan berlanjut. Kedua, bahan tereduksi dapat mereduksi oksigen menjadi superoksida atau peroksida merupakan radikal hidroksil dalam reaksi auto-oksidasi. Ascorbat dan asam urat dapat berfungsi sebagai anti oksidan, ikut serta secara langsung dalam auto-oksidasi, baik melalui reduksi aktifator oksigen lain seperti rangkaian logam transisi atau quinone, atau bertindak sebagai kofaktor enzim.
Proses tersebut dapat melibatkan kemampuan askorbat untuk depolimerisasi DNA, hambatan Na+/K+ ATPase otak, potensiasi toksisitas paraquat, dan sebagai mediator peroksidasi lemak. Juga mempunyai kontribusi kelainan patofisiologi dari metabolisme purin. Sifat yang sesungguhnya campuran pro atau antioksidan untuk bahan pereduksi khusus adalah integrasi kompleks dari beberapa faktor. Pada kasus zat pembersih radikal hidroksil, produk dari interaksi radikal dengan antioksidan umumnya kurang reaktif dibanding radikal hidroksil. Radikal yang terbentuk tersebut cukup stabil dan dalam konsentrasi cukup tinggi namun dapat terjadi mekanisme seperti pada glutation dan superoksida. pH sangat mempengaruhi reduksi langsung oksigen menjadi superoksida oleh senyawa sulfidril, sedangkan faktor lokal lainnya seperti konsentrasi molar dari molekul oksigen juga punya peranan penting.
Oksigen singlet dan bagian triplet molekul yang tereksitasi mungkin disempurnakan
melalui interaksi bersama sistem konjugasi sistem diene seperti yang ditemukan pada karoten, tokoferol, atau melanin. Seperti antioksidan pereduksi, senyawa tersebut dapat juga menghasilkan jenis elektron aktif dan mungkin juga penyakit.
Sebenarnya radikal bebas atau sering disebut oksidan merupakan molekul-molekul yang sangat reaktif di dalam tubuh dan pada hakikatnya dapat merusak bio molekul penting di dalam sel-sel, termasuk DNA. Hal ini merupakan penyebab utama penyakit serius seperti serangan jantung, kanser dan penuaan awal.
Berdasarkan penelitian saintis Moses Gomberg dan saintis lainnya, istilah radikal bebas dimaksudkan sebagai molekul yang relatif tidak stabil di dalam sel, mempunyai satu atau lebih elektron yang tidak berpasangan di orbit luarnya. Molekul tersebut bersifat reaktif dalam mencari pasangan elektronnya, yang biasanya “dicuri” dari sel tubuh lain. Hal inilah yang merosakkan sel-sel tubuh, sehingga terjadi penuaan awal.
Radikal bebas yang bersifat reaktif tersebut juga dapat menimbulkan perubahan kimia dan merosakkan pelbagai komponen sel hidup seperti protein, lipid, karbohidrat, dan asid nukleik. Lebih teruk lagi, jika radikal bebas sudah terbentuk dalam tubuh maka akan terjadi reaksi berantai dan menghasilkan radikal bebas baru yang akhirnya jumlahnya terus bertambah.
Zat anti oksidan adalah bahan yang dapat meneutralkan atau menghancurkan radikal bebas. Radikal bebas merupakan jenis oksigen yang memiliki tingkat reaktif yang tinggi dan secara semulajadi ada di dalam tubuh sebagai hasil dari reaksi biokimia di dalam tubuh. Radikal bebas juga terdapat di lingkungan sekitar kita yang berasal dari pencemaran udara, asap tembakau, pengewapan alkohol yang berlebihan, bahan pengawet, sinar Ultra Violet, X-rays, dan ozon. Radikal bebas dapat merosakkan sel tubuh apabila tubuh kekurangan zat anti oksidan atau bila terdapat radikal bebas berlebihan dalam tubuh. Hal ini dapat menyebabkan berkembangnya sel kanser, penyakit hati, arthritis, katarak, dan penyakit degeneratif lainnya, bahkan juga mempercepat proses penuaan.
Penyebab
Sinar ultraviolet matahari antara pukul 10.00 pagi – 3.00 petang, pencemaran asap rokok, alkohol, pembebasan asap kendaraan bermotor adalah faktor luaran yang memacu pembentukan radikal bebas di dalam tubuh. Setiap kali bernafas dengan menghirup oksigen pasti terjadi pengoksidaan yang menghasilkan sisa-sisa oksida yang disebut oksidan. Oksidan inilah yang juga membentuk radikal bebas .
Selain itu, gizi berlebihan merupakan faktor dalaman pembentukan radikal bebas dalam tubuh. Dalam makanan kita sehari-hari sebaiknya tidak berlebihan lemak, vitamin, protein, dan sebagainya kerana ketika tubuh kita mencerna makanan, selain menghasilkan tenaga, tubuh juga menghasilkan radikal bebas sebagai sebahagian dari proses metabolisme tubuh.
Stres oksidatif adalah ketidakseimbangan antara radikal bebas dan antioksidan yang dipicu oleh dua keadaan umum yakni kurangnya antioksidan, dan berlebihan produksi radikal bebas. Keadaan stres oksidatif membawa pada kerosakan oksidatif mulai dari tingkat sel, jaringan hingga ke organ tubuh, menyebabkan terjadinya percepatan proses penuaan dan munculnya penyakit. Berbagai penyakit yang telah diteliti dan didapati kuat berkaitan dengan aktiviti radikal bebas antara lain adalah stroke, asma, diabetes melitus, radang usus, penyumbatan kronik pembuluh darah di jantung, parkinson, hingga AIDS.
Teori penuaan dan radikal bebas pertama kali dikemukakan oleh Denham Harman dari University of Nebraska Medical Center di Omaha, AS pada 1956 yang menyatakan bahawa tubuh mengalami penuaan kerana serangan oksidasi dari zat-zat perosak. Kanser dan tumor telah sipersetujui oleh saintis sebagai penyakit yang berawal dari mutasi gen atau DNA sel. Radikal bebas jelas berperanan pada proses mutasi ini. Bahaya lainnya adalah bila bereaksi dengan low-density lipoprotein (LDL)-cholesterol menjadi bentuk yang reaktif sebagai faktor risiko penyakit jantung.
Radikal bebas (oksidan) ini boleh diatasi dengan mencegah kemasukan oksidan ini ke tubuh dengan memakai pelindung matahari di kulit, dan juga dengan antioksidan. Antioksidan dalam tubuh dapat memberikan perlindungan pada tubuh dari ancaman radikal bebas dan berfungsi untuk meneutralkannya. Manfaatnya dapat memperlambat proses penuaan dan mencegah berbagai penyakit di atas.
Makanan yang Mengandung Oksidan (Radikal Bebas)
Jenis makanan tertentu seperti fast food (makanan segera) berpotensi meninggalkan racun dalam tubuh, sebab jenis makanan ini mengandungi lemak dan bahan pengawet yang tinggi. Padahal untuk zaman sekarang kebiasaan makan makanan berlemak tinggi menjadi sesuatu yang sukar dielakkan kerana perubahan pola hidup masyarakat, khususnya di bandar besar.
Pegawai perubatan dan nutrisi menyebut makanan berlemak boleh menjadi sumber radikal bebas dalam tubuh. Menurut Prof Dr Harijono KS, SpKK, dekan Fakultas Kedoktoran UNS, radikal bebas ini berbahaya kerana amat reaktif mencari pasangan elektronnya. Jika radikal bebas sudah terbentuk dalam tubuh maka akan terjadi reaksi berantai dan menghasilkan radikal bebas baru yang akhirnya jumlahnya terus bertambah. Selanjutnya akan menyerang sel-sel tubuh kita sehingga terjadilah kerosakan pada sistem peredaran yang akan mempercepat proses penuaan.
Makanan yang Mengandung Antioksidan
Ada beberapa makanan yang merupakan sumber antikosidan, iaitu makanan yang mengandung Vitamin A, C, E, melantonin, betakaroteno seperti sayuran, kacang-kacangan, jagung, dan buah. Saat ini juga tersedia suplemen dan susu yang mengandung antioksidan. Daging mengandung banyak oksidan, jadi sebaiknya perbanyakkan memakan sayur dan buah.
Visualisasi anti oksidan melawan radikal bebas dapat dilihat pada
https://youtu.be/Ua_rrllQwJo
Masalah :
Mengapa Suatu bahan yang elektron lapisan luarnya penuh tidak akan terjadi reaksi kimia?
Bagaimana hubungan antioksidan dan radikal bebas?
Visualisasi anti oksidan melawan radikal bebas dapat dilihat pada
https://youtu.be/Ua_rrllQwJo
Masalah :
Mengapa Suatu bahan yang elektron lapisan luarnya penuh tidak akan terjadi reaksi kimia?
Bagaimana hubungan antioksidan dan radikal bebas?
DAFTAR PUSTAKA
http://www.avkimia.com/2017/06/reaksi-radikal-bebas-pada-klorinasi-metana.html
http://digilib.itb.ac.id/files/disk1/553/jbptitbpp-gdl-rizkisitin-27615-2-2007ta-1.pdf
http://www.noraihanqusyairi.com/2014/12/radikal-bebas-oksidan-dan-anti-oksidan.html
http://www.prosesdetox.com/pengertian-dan-bahaya-radikal-bebas-bagi-tubuh/
http://debimutiara.blogspot.co.id/2013/12/
https://youtu.be/Ua_rrllQwJo

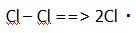




Mengapa Suatu bahan yang elektron lapisan luarnya penuh tidak akan terjadi reaksi kimia?
BalasHapusHal itu dikarenakan pada bahan yang elektron lapisan luarnya penuh telah terjadi kestabilan sehingga tidak bereaksi dengan zat lain lagi.
HapusMengapa padaPada radikal bebas elektron yang tidak berpasangan tidak mempengaruhi muatan elektrik dari molekulnya, dapat bermuatan positif, negatif, atau netral.?
BalasHapusPada radikal bebas elektron yang tidak berpasangan tidak mempengaruhi muatan elektrik dari molekulnya, dapat bermuatan positif, negatif, atau netral sehingga sering kali mencapai titik kestabilan. Sebagai molekul tidak stabil, radikal bebas selalu berusaha “menyerobot” elektron molekul lain di dalam tubuh untuk membuatnya stabil kembali. Hal ini dapat menghancurkan bangunan dan struktur sel-sel tubuh serta mengubah ukuran dan bentuk mereka. Bayangkanlah proses perusakan sel ini seperti perkaratan besi oleh oksigen yang menghancurkan bentuknya.
HapusJadi alasan mengapa pada radikal bebas elektron yang tidak berpasangan tidak mempengaruhi muatan elektrik dari molekulnya, dapat bermuatan positif, negatif, atau netral, hal ini dikarenakan radikal bebas tersebut sibuk menstabilkan dirinya sendiri dengan mencuri molekul dari zat lain.
mengapa Zat anti oksidan dikatakan bahan yang dapat meneutralkan atau menghancurkan radikal bebas?
BalasHapusBiasanya, tubuh memiliki sistem pertahanan alami untuk menetralisir radikal bebas agar tidak berkembang menjadi berbahaya. Namun, pengaruh lingkungan dan kebiasaan buruk seperti radiasi ultraviolet, polusi, kebiasaan mengkonsumsi “junk food” dan merokok, dapat membuat sistem pertahanan tubuh kewalahan menghadapi radikal bebas yang berjumlah besar.
HapusMengkonsumsi lebih banyak antioksidan membantu tubuh untuk menetralisir radikal bebas berbahaya. Antioksidan berperan menetralisir radikal bebas dengan “menyumbangkan” elektron sehingga membuatnya stabil. Diperkirakan ada lebih dari 4.000 senyawa dalam makanan yang berfungsi sebagai antioksidan. Yang paling banyak dipelajari adalah beta karoten (pro vitamin A), vitamin C, vitamin E, asam fenolik, selenium, klorofil, karotenoid, flavonoid, glutasion, koenzim Q10, melatonin dan likopen. Perlu dicatat bahwa vitamin A sendiri bukan antioksidan.
Selamat siang sdri Martha, saya ingin bertanya. Bisakah Anda menjelaskan hubungan antara radikal bebas dengan antioksidan?
BalasHapusAntioksidan dapat didefinisikan sebagai suatu zat yang dapat menghambat atau memperlambat proses oksidasi. Oksidasi adalah jenis reaksi kimia yang melibatkan pengikatan oksigen, pelepasan hydrogen, atau pelepasan elektron. Proses oksidasi adalah peristiwa alami yang terjadi di alam dan dapat terjadi dimana-mana tak terkecuali di dalam tubuh kita.
HapusAntioksidan ini secara nyata mampu memperlambat atau menghambat oksidasi zat yang mudah teroksidasi meskipun dalam konsentrasi rendah. Antioksidan juga sesuai didefinisikan sebagai senyawa-senyawa yang melindungi sel dari efek berbahaya radikal bebas oksigen reaktif jika berkaitan dengan penyakit, radikal bebas ini dapat berasal dari metabolisme tubuh maupun faktor eksternal lainnya.
adikal bebas adalah atom / molekul yang memiliki elektron tidak berpasangan di bagian orbital yang terluar serta mampu berdiri sendiri. Pada umumnya mekanisme reaksi radikal bebas dalam tubuh terjadi dengan cepat bersama atom yang lain untuk mengisi orbital yang kosong. Simbol penulisan radikal bebas adalah berupa titik yang terdapat di penulisan atom / molekul.
HapusPengertian Reactive Oxygen Species (ROS) adalah radikal bebas yang berupa oksigen dan turunannya yang sangat reaktif. Radikal bebas tersebut dapat menyebabkan kerusakan oksidatif terhadap molekul protein, DNA, lemak membran sel, dan komponen sel atau jaringan yang lain, oleh karena itu Reactive Oxygen Species (ROS) memiliki satu atau lebih atom yang tidak berpasangan. Reactive Oxygen Species (ROS) dihasilkan pada saat terjadinya metabolisme oksidatif dalam tubuh seperti proses oksidasi makanan menjadi energi.
Bagaimana cara menentukan struktur kimia radikal bebas??
BalasHapusRadikal bebas dapat terbentuk in-vivo dan in-vitro secara :
Hapus1. Pemecahan satu molekul normal secara homolitik menjadi dua. Proses ini jarang
terjadi pada sistem biologi karena memerlukan tenaga yang tinggi dari sinar
ultraviolet, panas, dan radiasi ion.
2. Kehilangan satu elektron dari molekul normal
3. Penambahan elektron pada molekul normal
Pada radikal bebas elektron yang tidak berpasangan tidak mempengaruhi muatan elektrik dari molekulnya, dapat bermuatan positif, negatif, atau netral.
Jadi, bila ada suatu molekul yang memiliki ciri-ciri tersebut, dapat dikatakan bahwa molekul tersebut merupakan struktur molekul dari radikal bebas.
radikal bebas adalah suatu atom atau molekul yang tidak stabil dan sangat reaktif karena memiliki satu atau lebih elektron yang tidak berpasangan pada orbital terluarnya.Antioksidan adalah senyawa yang mampu menangkal atau meredam efek negatif oksidan dalam tubuh, bekerja dengan cara mendonorkan satu elektronnya kepada senyawa yang bersifat oksidan sehingga aktifitas senyawa oksidan tersebut dapat dihambat.
BalasHapusAntioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya cuma- cuma kepada molekul radikal bebas tanpa terganggu sama sekali fungsinya dan dapat memutus reaksi berantai dari radikal bebas.
Saya akan membantu menjawab permasalahan anda,Sebetulnya radikal bebas atau sering disebut oksidan merupakan molekul-molekul yang sangat reaktif di dalam tubuh dan pada hakekatnya dapat merusak bio molekul penting di dalam sel-sel, termasuk DNA. Hal ini merupakan penyebab utama penyakit fatal seperti serangan jantung, kanker hingga penuaan dini.
BalasHapusBerdasarkan penelitian ilmuwan Moses Gomberg dan ilmuwan lainnya, istilah radikal bebas diartikan sebagai molekul yang relatif tidak stabil di dalam sel, mempunyai satu atau lebih elektron yang tidak berpasangan di orbit luarnya. Molekul tersebut bersifat reaktif dalam mencari pasangan elektronnya, yang biasanya “dicuri” dari sel tubuh lain. Hal inilah yang merusak sel-sel tubuh, sehingga berujung pada penuaan dini.
Saya akan membantu menjawab permasalahan anda,Sebetulnya radikal bebas atau sering disebut oksidan merupakan molekul-molekul yang sangat reaktif di dalam tubuh dan pada hakekatnya dapat merusak bio molekul penting di dalam sel-sel, termasuk DNA. Hal ini merupakan penyebab utama penyakit fatal seperti serangan jantung, kanker hingga penuaan dini.
BalasHapusBerdasarkan penelitian ilmuwan Moses Gomberg dan ilmuwan lainnya, istilah radikal bebas diartikan sebagai molekul yang relatif tidak stabil di dalam sel, mempunyai satu atau lebih elektron yang tidak berpasangan di orbit luarnya. Molekul tersebut bersifat reaktif dalam mencari pasangan elektronnya, yang biasanya “dicuri” dari sel tubuh lain. Hal inilah yang merusak sel-sel tubuh, sehingga berujung pada penuaan dini.
Reaksi yang lengkap pada tingkat molekul yang dapat menimbulkan Radikal bebas atau oksidator kuat akibat tubuh terkena radiasi sehingga mengganggu kerja metabolisme seperti terganggunya aktivitas enzim. Contohnya: proses ionisasi air yang terganggu
BalasHapus